Obat Antiinflamasi NonSteroid(OAINS) :
KAFLAM (Natrium Diklofenak)
Disusun oleh :
Veronica Desi R (068114092)
Tania Gunawan (068114121)
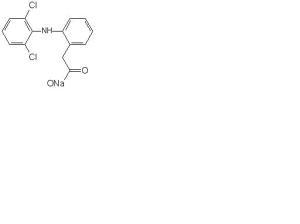
Farmakologi dan farmakokinetika
KAFLAM adalah obat antiinflamasi nonsteroid yang mengandung garam kalium dari diklofenak. Obat ini memiliki efek analgesic dan antiinflamasi.
Mekanisme kerjanya adalah dengan menghambat sintesis prostaglandin, mediator yang berperan penting dalam proses terjadinya inflamasi, nyeri dan demam. Kalium diklofenak akan diabsorbsi dengan cepat dan lengkap dan jumlah yang diabsorbsi tidak berkurang jika diberikan bersama dengan makanan. Kadar puncak obat dicapai dalam ½ -1 jam. Ikatan protein 99,7%, waktu paruh 1-2 jam. Pemberian dosis berulang tiidak menyebabkan akumulasi . eliminasi terutama melalui urin
Natrium diklofenak dalam bentuk CR/lepas-lambat terkendali adalah salah satu tekonologi yang dikembangkan untuk memperbaiki efikasi dan toleransi diklofenak. Pengembangan formulasi yang canggih dengan teknologi tinggi pada “drug delivery System” telah dilakukan oleh Klinge Pharma GmbH dan telah dipasarkan di Indonesia dengan nama Deflamat CR oleh PT. Actavis Indonesia. Deflamat CR (gabungan antara teknologi Enteric-Coated dengan Sustained-Release ) memiliki bentuk yang unik yaitu pelet CR dimana zak aktif terbagi dalam ratusan unit sferis kecil ( pelet) yang akan menjamin penyebaran yang baik dari zat aktif diseluruh saluran gastro-intestinal sehingga akan memperbaiki toleransi gastro-intestinal dari obat AINS
Selain itu, dengan ukuran partikel yang kecil, pelet bisa melintasi pilorus dengan cepat bersama kimus, dimana transportasi menuju doudenum tidak bergantung pada pengosongan lambung, sehingga waktu transit obat rata-rata lebih cepat dan dengan sistem pelepasannya yang terkendali, absorpsi yang cepat dan kontinyu memberikan kontribusi utama untuk memperbaiki bioavilabilitas obat AINS.
Beberapa studi klinis natrium diklofenak yang diberikan sebagai monoterapi atau kombinasi, menunjukkan obat ini efektif meredakan gejala osteoartritis (OA) maupun reumatoid artritis (RA). Studi yang dilakukan di Jerman terhadap 230 pasien menunjukkan, penggunaan diklofenak dalam sediaan gel untuk pasien osteoartritis pada lulut terbukti efektif dan aman untuk meredakan gejala osteoartritis pada lutut. Studi ini dimuat dalam Journal of Rheumatology
Indikasi
Sebagai pengobatan jangka pendek untuk kondisi-kondisi akut sebagai berikut:
– Nyeri inflamasi setelah trauma seperti terkilir.
– Nyeri dan inflamasi setelah operasi, seperti operasi gigi atau tulang.
Sebagai adjuvant pada nyeri inflamsi yang berat dari infeksi telinga, hidung, atau tenggorokan misalnya tonsilofaringitis, otitis.
Sesuai dengan prinsip pengobatan umum, penyakitnya sendiri harus diobati dengan terapi dasar. Demam sendiri bukan suatu indikasi.
Kontraindikasi
Hipersensitif terhadap zat aktif dan tukak lambung. Juga dikontraindikasikan pada pasien dengan riwayat tercetusnya serangan asma, urtikaria atau rhinitis akut akibat obat-obat anti nonsteroid lainnya
Peringatan dan perhatian
– Hati-hati penggunaan pada penderita dekomposisi jantung atau hipertensi, karena diklofenak dapat menyebabkan retensi cairan dan edema.
– Hati-hati penggunaan pada penderita gangguan fungsi ginjal, jantung, hati, penderita usia lanjut dan penderita dengan luka atau perdarahan pada saluran pencernaan.
– Hindarkan penggunaan pada penderita porfiria hati.
-Hati-hati penggunaan selama kehamilan karena diklofenak dapat menembus plasenta.
– Diklofenak tidak dianjurkan untuk ibu menyusui karena diklofenak diekskresikan melalui ASI.
– Pada anak-anak efektivitas dan keamanannya belum diketahui dengan pasti.
Efek samping
Saluran pencernaan :
– Kadang- kadang : nyeri epigastrum, gangguan saluran pencernaan seperti mual, muntah, diare, kejang perut, dyspepsia, perut kembung, anoreksia.
– Jarang : perdarahan saluran pencernaan ( hematemesis, melena, tukak lambung dengan atau tanpa perdarahan/ perforasi, diare berdarah )
– Sangat jarang : gangguan usus bawah seperti “nonspesifik haemorrhagic colitis” dan eksaserbasi colitis ulseratif atau chron’s disease, stomatitis aphthosa, glositis, lesi esophagus, konstipasi.
Saluran saraf pusat dan perifer :
– Kadang- kadang : sakit kepala, pusing, vertigo
– Jarang : perasaan ngantuk
– Sangat jarang : gangguan sensasi ternasuk parestesia, gangguan memori, disorientasi, gangguan penhlihatan ( blurred vision, diplopia ), gangguan pendengaran, tinnitus, insomnia, iritabilitas, kejang, depresi, kecemasan,mimpi buruk, tremor, reaksi psikotik, gangguan perubahan rasa.
Kulit
– Kadang-kadang : ruam atau erupsi kulit
– Jarang : urtikaria
– Sangat jarang : erupsi bulosa , eksema, eritema multiforme, SSJ, lyell syndrome ( epidermolisis toksik akut ), eritrodema ( dermatitis exfoliatif ), rambut rontok, reaksi fotosensitivitas, purpura termasuk purpura alergik
Sistem urogenital, fungsi hati, darah, hipersensitivitas, susunan organ lainnya.
Interaksi obat
Apabila diberikan bersamaan dengan preparat yang mengandung lithium atau digoxin, kadar obat-obat tersebut dalam plasma meningkat tetapi tidak dijumpai adanya gejala kelebihan dosis.
Beberapa obat antiinflamasi nonsteroid dapat menghambat aktivitas dari diuretika. Pengobatan bersamaan dengan diuretika golongan hemat kalium mungkin mungkin disertai dengan kenaikan kadar kalium dalam serum.
Pemberian bersamaan dengan antiinflamasi nonsteroid sistemik dapat menambah terjadinya efek samping. Meskipun pada uji klinik diklofenak tidak mempengaruhi efek antikoagulan, sangat jarang dilaporkan adanya penambahan resiko perdarahan dengan kombinasi diklofenak dan antikoagulan, oleh karena itu dianjrkan untuk dilakukan pemantauan yang ketat terhadap pasien tersebut. Seperti dengan anti inflamasi nonsteroid lainnya, diklofenak dalam dosis tinggi (200 mg ) dapat menghambat agrregasi platelet untuk sementara.
Uji klinik memperlihatkan bahwa diklofenak dapat diberikan bersamaan dengan anti diabetic oral tanpa mempengaruhi efek klinis dari masing-masing obat. Sangat jarang dilaporkan efek hipoglikemik dan hiperglikemik dengan adanya diklofenak sehingga diperlukan penyesuaian dosis obat-obat hipoglikemik. Perhatian harus diberikan bila antiinflamasi nonsteroid diberikan kurang dari 24 jam sebelum atau setelah pengobatan dengan methotrexate dalam darah dapat meningkat dan toksisitas dari pbat ini bertambah.
Penambahan nefrotoksisitas cyclosporine munkin terjadi oleh karena efek obat-obat antiinflamasi nonsteroid terhadap prostaglandin ginjal.
Dosis berlebih
Penanganan keracunan akut dengan antiinflamasi nonsteroid pada dasrnya dilakukan dengan tindakan supportif dan simptomatik. Tidak ada gambaran klinis yang khas dari dosis berlebih diklofenak. Tindakan pengobatan yang dilakukan dalam hal dosis berlebih adalah sebagai erikut : absorbs harus dicegah segera setelah dosis berlebih dengan pencucian lambungdan pengobatan dengan arang aktif. Pegobatan suportif dan simptomatik harus diberikan untuk komplikasi seperti hipotensi, gagal ginjal, kejang, iritasi saluran pencernaan dan depresi pernapasan. Tetapi spesifik seperti “ forced dieresis”, dialysis atau hemoperfusi mungkin tidak membantu menghilangkan antirematik non steroid karena jumlah ikatan protein yang tinggi.
Dosis
Umumnya takaran permulaan untuk dewasa 100-150 mg sehari. Pada kasus-kasus yang sedang , juga untuk anak-anak di atas usia 14 tahun 75-100 mg sehari pada umumnya sudah mencukupi.
Dosis seharian harus diberikan dengan dosis terbagi 2-3 kali
Tablet harus diberikan dengan air, sebaiknya sebelum makan, tidak dianjurkan untuk pemakaian anak-anak.
Daftar pustaka
Neal,M.J., 2006, Farmakologi Medis, 70-71, Erlangga, Jakarta
www.narod-sobe.cz/…/ChemPict.htm
http://www.majalah-farmacia.com/rubrik/one_news.asp?IDNews=181.









